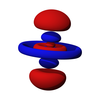
sp3杂化
外观
(重定向自Sp3混成)
| sp3杂化 | |
|---|---|
| sp3杂化后的电子轨道排布 (以碳元素为例) | |
| 参与sp3杂化的原子轨道 | |
| s轨道 | 1个 |
| p轨道 | 3个 |
| 含有采用sp3杂化原子的分子或离子 | |
| B | B2Cl6 |
| C | CH4 |
| N | NH3 |
| O | H2O、H2O2 |
| S | SO42- |
sp3杂化(英語:sp3 hybridization)是指一个原子同一电子层内由一个ns轨道和三个np轨道发生杂化的过程。原子发生sp3杂化后,上述ns轨道和np轨道便会转化成为四个等价的原子轨道,称为“sp3杂化轨道”。四个sp3杂化轨道的对称轴两两之间的夹角相同,皆为109°28'。sp3杂化一般发生在分子形成过程中。杂化发生前,原子最外层s轨道中的一个电子被激发至p轨道,使将要发生杂化的原子进入激发态;之后,该层的s轨道与三个p轨道发生杂化。此过程中,能量相近的s轨道和p轨道发生叠加,不同类型的原子轨道重新分配能量并调整方向。
以碳原子为例:处于基态的碳原子(电子排布式为:1s22s22p2)的一个2s电子激发至一个空的2p轨道上,使原子进入激发态(电子排布式为:1s22s12p3)。然后,一个2s轨道再和上述三个各填充了一个电子的2p轨道进行sp3杂化,形成四个sp3杂化轨道。该过程中碳原子的原子轨道排布变化情况如下图所示:
在有机化学中,碳原子与其他原子以单键连接时(如烷烃、环烷烃中的碳碳单键和碳氢单键等),碳原子均采用sp3杂化形式。[1]
参考文献
[编辑]- ^ 孔祥文等. 《有机化学》. 北京: 化学工业出版社. 2010年2月: 35 [2012-01-20]. ISBN 978-7-122-07037-1. (原始内容存档于2019-02-17) (中文).
| |||||||||||||||||||||||||||||||