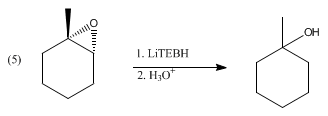三乙基硼氫化鋰
外觀
| 三乙基硼氫化鋰 | |
|---|---|

| |
| IUPAC名 Lithium triethylboranuide | |
| 別名 | Superhydride LiTEBH |
| 識別 | |
| CAS編號 | 22560-16-3 |
| PubChem | 23712863 |
| ChemSpider | 2006168 |
| SMILES |
|
| 性質 | |
| 化學式 | Li(C2H5)3BH |
| 摩爾質量 | 105.95 g/mol g·mol⁻¹ |
| 外觀 | 無色至黃色液體 |
| 密度 | 0.890 g/cm3,液體 |
| 沸點 | 66 °C(339 K) |
| 溶解性(水) | 活潑 |
| 危險性 | |
GHS危險性符號  
| |
| GHS提示詞 | Danger |
| H-術語 | H250, H260, H314, H335 |
| P-術語 | P210, P222, P223, P231+232, P260, P261, P264, P271, P280, P301+330+331, P302+334, P303+361+353, P304+340, P305+351+338 |
| 主要危害 | 易燃 腐蝕性 引致灼傷 疑似致癌物 |
| NFPA 704 | |
| 相關物質 | |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
三乙基硼氫化鋰是一種有機硼化合物,化學式為LiEt3BH。它有LiTEBH或Superhydride之稱,是強還原劑,用於有機金屬化學和有機化學。它是無色或白色液體,但通常以四氫呋喃溶液形式銷售並使用。[1]有關的還原劑包括三乙基硼氫化鈉,可它以以甲苯溶液形式購買。
製備
[編輯]氫化鋰(LiH)和三乙基硼烷(Et3B)在四氫呋喃裏反應,可以生成LiBHEt3:
- LiH + Et3B → LiEt3BH
它的四氫呋喃溶液如不遇水分和空氣,可以長期保持穩定。
反應
[編輯]LiBHEt3可以還原各種各樣的官能基,但在氫化物試劑中,它並不是例外。LiBHEt3反而留給難以還原的受體使用,例如有位阻的羰基,如下圖所示2,2,4,4-四甲基-3-戊酮的還原。在其他情況下,它可以將酸酐還原成醇和羧酸,而非二元醇。同樣地,它可以將內酯還原成二元醇。α,β-內酯會經過1,4-加成反應,生成鋰烯醇化物。二硫化物會(通過硫醇鹽)被還原成硫醇。LiBHEt3可以將羧酸去質子化,但不能還原所生成的鋰羧酸鹽。同樣道理,環氧化物遇LiBHEt3時會經過開環反應,生成醇。如果環氧化物不對稱,反應可以具有高區域選擇性和立體選擇性而進行,傾向於在最不位阻的位置進攻:
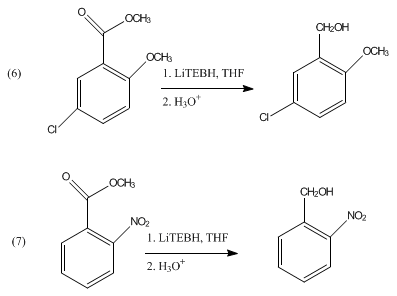
LiBHEt3不可以還原縮醛和縮酮。LiBHEt3可用於甲磺酸酯和甲苯磺酸酯的還原裂解。[4]LiBHEt3可以將三級N-酰基基團選擇性去保護,也不會影響二級胺的官能度。[5]據研究顯示,它也可以將芳香酯還原成對應的醇(反應6、7)。
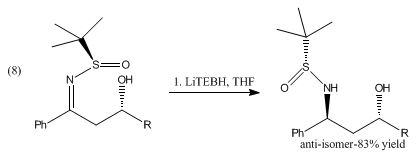
LiBHEt3也可以將吡啶和異喹啉分別還原成哌啶和四氫異喹啉。[6]鄰苯二酚硼烷和LiBHEt3還原β-羥基亞磺酰基亞胺還原,可以生成anti-1,3-氨基醇(反應8)。[7]
預防措施
[編輯]LiBHEt3遇水、醇或酸會發生劇烈的放熱反應,生成氫氣和自燃的三乙基硼烷。[1]
參考文獻
[編輯]- ^ 1.0 1.1 1.2 Zaidlewicz, M.; Brown, H.C. Lithium Triethylborohydride. Encyclopedia of Reagents for Organic Synthesis. John Wiley & Sons. 2001 [2022-02-18]. ISBN 0471936235. doi:10.1002/047084289X.rl148.
- ^ Marek Zaidlewicz; Herbert C. Brown. Lithium Triethylborohydride. Encyclopedia of Reagents for Organic Synthesis. 2001. ISBN 0471936235. doi:10.1002/047084289X.rl148.
- ^ Brown, H.C.; Kim, S.C.; Krishnamurthy, S. Selective reductions. 27. Reaction of alkyl halides with representative complex metal hydrides and metal hydrides. Comparison of various hydride reducing agents. J. Org. Chem. 1980-02-01, 45 (5): 849–856 [2022-02-18]. doi:10.1021/jo01293a018.
- ^ Baer, H.H.; Mekarska-Falicki, M. Stereochemical dependence of the mechanism of deoxygenation, with lithium triethylborohydride, in 4,6-O-benzylidenehexopyranoside p-toluenesulfonates. Canadian Journal of Chemistry. November 1985, 63 (11): 3043 [2022-02-18]. doi:10.1139/v85-505.
- ^ Tanaka, H.; Ogasawara, K. Utilization oh lithium triethylborohydride as a selective N-acyl deprotecting agent. Tetrahedron Lett. 2002-06-17, 43 (25): 4417 [2022-02-18]. doi:10.1016/S0040-4039(02)00844-4.
- ^ Blough, B.E.; Carroll, F.I. Reduction of isoquinoline and pyridine-containing heterocycles with lithium triethylborohydride (Super-Hydride®). Tetrahedron Lett. 1993-11-05, 34 (45): 7239 [2022-02-18]. doi:10.1016/S0040-4039(00)79297-5.
- ^ Kochi, T.; Tang, T.P.; Ellman, J.A. Asymmetric Synthesis of syn- and anti-1,3-Amino Alcohols. J. Am. Chem. Soc. 2002-05-14, 124 (23): 6518–6519 [2022-02-18]. PMID 12047156. doi:10.1021/ja026292g.